Alginate de Sodium/Bicarbonate de Sodium Mylan Viatris 500 mg/267 mg Sachets x 24
Médicament - AllopathieCe médicament est indiqué dans le traitement symptomatique du reflux gastro-oesophagien. En savoir +
- Femme enceinte ? Autorisé
- Allaitement ? Autorisé
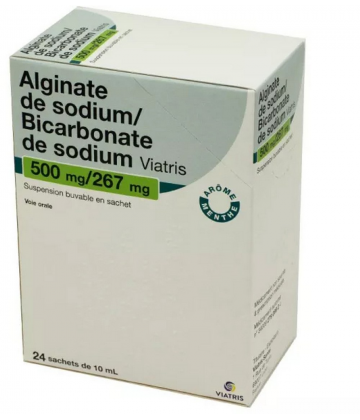
L'Alginate de Sodium/Bicarbonate de Sodium Viatris est un médicament destiné à soulager les maux d'estomac, notamment les brûlures et les remontées acides.
Les informations à connaître sur l'Alginate de Sodium/Bicarbonate de Sodium Viatris
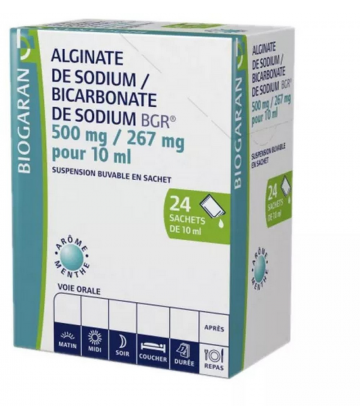
L'Alginate de Sodium/Bicarbonate de Sodium Viatris se présente sous forme de sachets contenant une suspension buvable.
Quelle est la posologie de l'Alginate de Sodium/Bicarbonate de Sodium Viatris
Il est recommandé de prendre 1 sachet 3 fois par jour après les 3 principaux repas et éventuellement une prise supplémentaire le soir au coucher.
Cette posologie peut être doublée à 2 sachets par prise en cas de reflux ou d'inflammation œsophagienne sévères.
Le contenu du sachet peut être avalé directement.
Les précautions d'emploi avec l'Alginate de Sodium/Bicarbonate de Sodium Viatris
Ce médicament ne doit pas être utilisé en cas d'allergie aux principes actifs ou à l'un des excipients.
Ce médicament contient 139 mg de sodium par sachet, cette quantité de sodium doit être prise en compte pour les patients devant suivre un régime sans sel. Ce médicament contient du parahydroxybenzoate de propyle et du parahydroxybenzoate de méthyle et peut provoquer des réactions allergiques (éventuellement retardées).
Ce médicament contient du calcium. Chaque sachet contient 160 mg de carbonate de calcium. Des précautions doivent être prises chez les patients présentant une hypercalcémie, une néphrocalcinose et ayant des calculs rénaux.
Par mesure de précaution, il est recommandé d'espacer les prises des autres médicaments et de l'Alginate de Sodium/Bicarbonate de Sodium Viatris d'au moins 2 heures. Ce médicament pourrait diminuer l'efficacité des autres médicaments.
L'Alginate de Sodium/Bicarbonate de Sodium peut provoquer des réactions allergiques et des effets respiratoires comme un bronchospasme.
Utilisation de l'Alginate de Sodium/Bicarbonate de Sodium pendant la grossesse et l'allaitement
Des études cliniques n’ont mis en évidence aucun effet malformatif, ni toxique des principes actifs pour le fœtus ou le nouveau-né. L'Alginate de Sodium/Bicarbonate de Sodium Viatris peut être utilisé pendant la grossesse si nécessaire.
Il en est de même pour l'allaitement.
L'avis de notre pharmacien sur l'Alginate de Sodium/Bicarbonate de Sodium Viatris
L'Alginate de Sodium/Bicarbonate de Sodium Viatris est le médicament générique de la spécialité Gaviscon en sachets. Ce médicament est couramment utilisé pour soulager les brûlures d'estomac et les remontées acides dans l'œsophage. Ce traitement permet d'améliorer les symptômes de brûlures, mais n'en soigne pas la cause. En l'absence d'amélioration de vos symptômes malgré l'utilisation du traitement, demandez conseil à votre médecin.
L'Alginate de Sodium/Bicarbonate de Sodium Viatris permet une amélioration immédiate des symptômes grâce à son effet pansement. Dans le cas de brûlures d'estomac chronique, il peut être associé à un traitement inhibiteur de la pompe à protons comme l'Oméprazole.
Sa forme en sachet individuel est pratique et peut être emmenée partout en se glissant facilement dans un sac à main.
Votre pharmacien vous conseille en vidéo !
Questions fréquemment posées sur l'Alginate de Sodium/Bicarbonate de Sodium Viatris
Les pharmaciens LaSante.net répondent à vos questions sur l'Alginate de Sodium/Bicarbonate de Sodium Viatris.
Quand puis-je prendre l'Alginate de Sodium/Bicarbonate de Sodium Viatris ?
Il est possible de prendre Alginate de Sodium/Bicarbonate de Sodium Viatris dès l'apparition des symptômes. Il est préférable de prendre ce médicament après les repas.
En combien de temps agit Alginate de Sodium/Bicarbonate de Sodium Viatris ?
Alginate de Sodium/Bicarbonate de Sodium Viatris agit en quelques minutes et soulage les symptômes de brûlures d'estomac.
Récapitulatif de Alginate de Sodium/Bicarbonate de Sodium Viatris
| Classe pharmacothérapeutique | autres médicaments pour l’ulcère peptique et le reflux gastro-œsophagien (R.G.O) |
|---|---|
| Code ATC | A02BX |
| Forme galénique | suspension buvable en sachet |
| Substance(s) active(s) | Alginate de sodium, Bicarbonate de sodium |
| Excipient(s) à effet notoire | sodium (139 mg par sachet), parahydroxybenzoate de méthyle (E218) (40 mg par sachet), parahydroxybenzoate de propyle (E216) (6 mg par sachet) |
| Modalités de prise | 1 sachet 3 fois par jour après les 3 principaux repas et éventuellement le soir au coucher |
| Contre indications | Allergie à l'un des composants du médicament |
| Effets indésirables | Réaction anaphylactique ou d'hypersensibilité, effets respiratoires tels que bronchospasme |
| Interactions médicamenteuses | Un délai de 2 heures doit être laissé entre la prise d'Alginate de Sodium/Bicarbonate de Sodium Viatris et les autres médicaments |
 Troubles de la digestion
Troubles de la digestion
Les troubles digestifs (constipation, diarrhée, ballonnements...) peuvent être définis comme un ensemble de symptômes liés au fonctionnement de l’appareil digestif et appelés communément les "maux de ventre". L'apparition de ces ...
 Reflux gastro-oesophagien
Reflux gastro-oesophagien
Le reflux gastro-oesophagien est une pathologie très fréquente et certainement sous-estimée puisqu'elle n'entraîne pas de consultation systématique. En France, on estime qu'une personne sur 5 est atteinte de reflux gastro-oesophagien (ou RGO). Et ...